カルボン酸は、カルボニルがヒドロキシル基に結合したカルボニル化合物です。当然のことですが、カルボキシルという名前はカルボニルとヒドロキシルの組み合わせを指します。カルボン酸は沸点の高い有機酸です。分子量が低いものは水にも溶けます。
これらの酸には、正式な命名法では接尾辞「-oic」が付き、その前に「酸」という単語を付ける必要があります。アミノ酸や脂肪酸の構成成分として存在するほか、多くの医薬品や化粧品の製造に使用されています。これらは非常に反応性が高く、塩基と反応するとカルボン酸の塩を形成します。
カルボン酸についてのまとめ
カルボン酸は、カルボニルの sp 2炭素がヒドロキシル基に結合したカルボニル化合物です。
カルボキシル基はカルボニルとヒドロキシルの結合部分です。
カルボン酸は有機酸であり、一部は水溶性が良く、沸点が高くなります。
Iupac は、カルボン酸の名前は「酸」で始まり、接尾辞「-oic」が付くと判断しています。
カルボン酸は主に化粧品や医薬品の製造に使用されます。
カルボン酸はアミノ酸や脂肪酸の一部です。
カルボン酸には多くの反応点があるため、多くの有機反応が起こります。
カルボン酸は塩基と反応するとカルボン酸塩を形成します。
カルボン酸の特徴
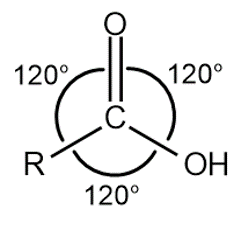
カルボン酸は、カルボニルの sp 2炭素がヒドロキシル (OH) に結合したカルボニル化合物です。カルボニル sp 2炭素のもう 1 つの結合は、アルキルまたは芳香族基 (R) と結合しており、カルボン酸が非環式化合物の間に配置されます。
「カルボキシル」という名前は、カルボニルとヒドロキシルの組み合わせに由来し、一般的にカルボキシルと呼ばれる基(カルボニル+ヒドロキシル)を名付けています。

sp 2ハイブリダイゼーションは、2 つの単結合 (2 つのシグマ結合、σ) と 1 つの二重結合 (1 つのシグマ結合、σ、および 1 つのパイ結合、π) を形成する炭素原子によって特徴付けられます。これに関連して、平らな三角形の幾何学形状では、カルボキシル基の結合間の角度が 120 ° であることがわかります。
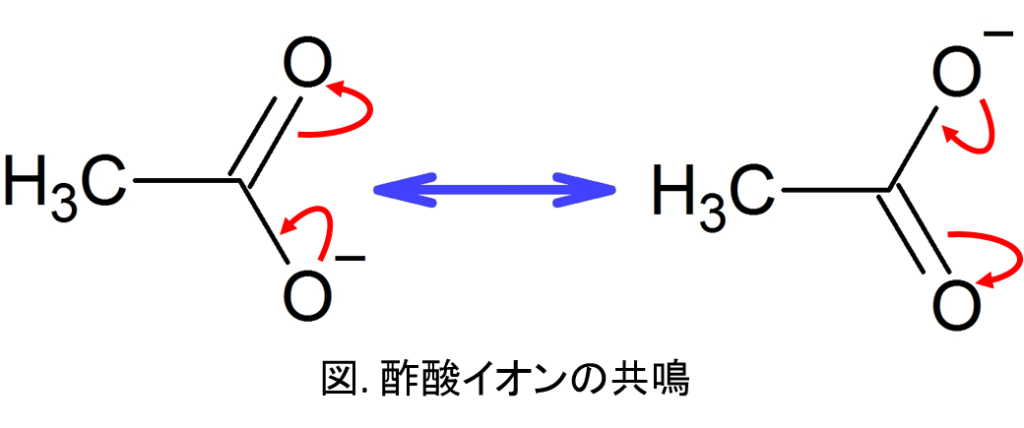
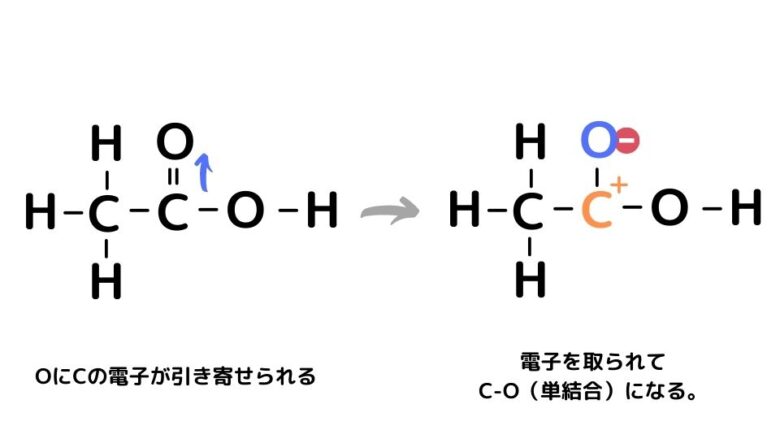
カルボン酸の主な特徴は酸性であることです。イオン化可能な水素は正確にはヒドロキシルの水素です。ただし、酸性度は R 鎖の性質によって影響されます (誘導効果)。
カルボン酸は極性物質であり、水に溶けます。水への溶解度に関するもう 1 つの重要な点は、カルボン酸分子がヒドロキシル基により水と水素結合を形成できることです。ただし、R 鎖が大きな非極性または弱い極性の性質を持っている場合、溶解度は低下します。
これらの酸は、2 つの分子間水素結合を形成することもあります。この配置により、そのような化合物は他の同様の化合物と比較して高い沸点を持つことができます。
カルボン酸の命名法
カルボン酸の体系的な命名法は、他の有機官能基と同様に、国際純粋応用化学連合 (Iupac) の規則によって定義されています。
カルボン酸の場合、接尾辞「-oic」に加えて、化合物名の前に「酸」という名前を使用することが確立されます。
一部のカルボン酸には、天然の起源を示すラテン語やギリシャ語に由来する一般的な (または俗っぽい) 名前が付いています。このような名前は、公式ではないにもかかわらず広く使用されており、強調する価値があります。
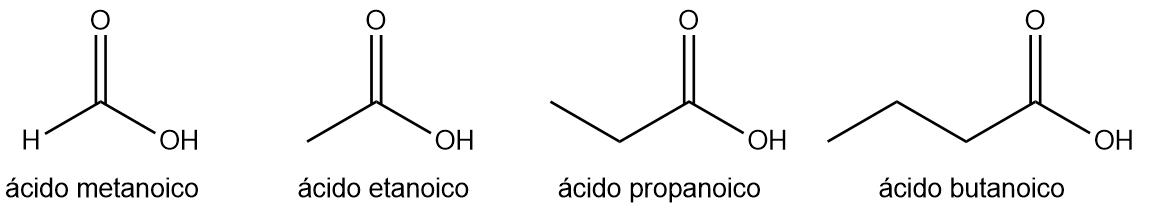
ギ酸 (メタン酸) : アリ、ミツバチ、その他の刺す昆虫に含まれています。名前はラテン語で「アリ」を意味する「 formica 」に由来しています。
酢酸(エタン酸) :酢に含まれており、アセタムはラテン語で「酢」と訳されます。
プロピオン酸 (プロパン酸) : 脂肪酸を指す特徴を持つ最小のカルボン酸で、その名前はギリシャ語のpro (「最初」) とpion (「脂肪」) に由来しています。
酪酸 (ブタン酸) : 腐ったバターの臭いの原因となり、その名前はラテン語で「バター」を意味するbutyrumに由来しています。
吉草酸(ペンタン酸):古代ギリシャ/ローマ帝国の時代から鎮静剤として使用されてきた多年草ハーブであるバレリアンに含まれています。
カプロン酸(ヘキサン酸) :ヤギの乳に含まれており、その臭いはヤギの特有の臭いに似ています。 Caperはラテン語で「ヤギ」を意味します。
一般名のうち広く使用されているのは、ギ酸と酢酸の 2 つだけです。学術書でもよく使われる言葉なので、暗記しておくと良いでしょう。カルボン酸の通常の命名法について詳しくは、ここをクリックしてください。
カルボン酸は何に分類されますか?
一般に、炭化水素の場合のように、カルボン酸には特定の分類がありません。ただし、無機酸と同様に、イオン化可能な水素の数に応じて分類できます。
カルボン酸のイオン化可能な水素はカルボキシルの水酸基にあるため、官能基の数は分類に役立ちます。
モノカルボン酸: カルボキシル基が 1 つだけあります。
ジカルボン酸: 2 つのカルボキシル基。
トリカルボン酸: 3 つのカルボキシル基。
等々。 2つ以上のカルボキシル基を有する酸をポリカルボン酸と呼ぶことができる。
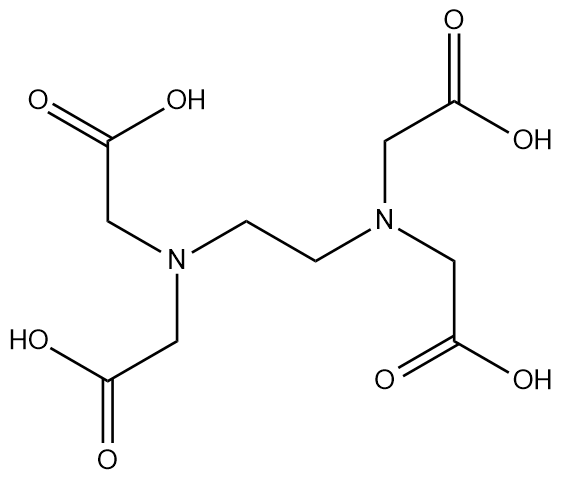
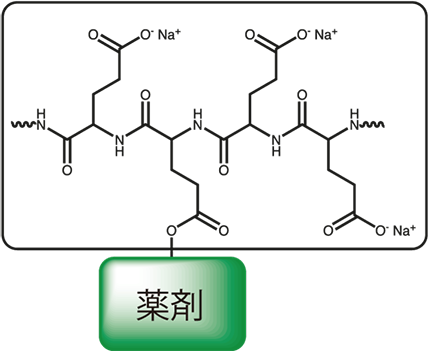
エチレンジアミン四酢酸 (EDTA) は、4 つのカルボキシル基を持つカルボン酸です。その構造は次のとおりです。
カルボン酸の応用
カルボン酸は私たちの体、健康、食事に大きく関係しています。アスピリン (アセチルサリチル酸)とイブプロフェン、広く商品化されている 2 つの薬剤は、その組成中にカルボン酸官能基を持っています。
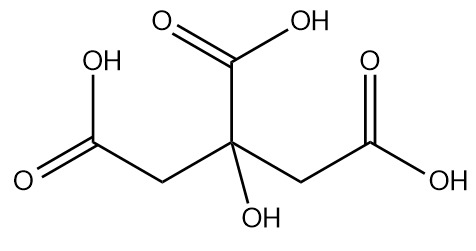
オレンジやレモンなどの果物に含まれるクエン酸は、酸度調整剤であることに加えて、抗酸化剤、酸味料、風味付け、封鎖特性などの複数の機能があるため、食品および飲料業界で最も使用されている酸です。言い換えれば、飲料や食品の風味を維持し、酸味を保証するために使用されるほか、pHを調整し、不快な味をマスキングし、甘味を中和するために使用されます。
BHA はニキビや脂性肌の治療に非常に効果的です。これらは皮膚の肥厚を軽減し、細菌や真菌による汚染を防ぎ、死んだ細胞や余分な油分を除去することで皮膚細胞を再生します。また、内部ニキビの治療に優れた抗炎症剤でもあります。顕著な BHA は、アセチルサリチル酸の前駆体であるサリチル酸です。 BHA は AHA と組み合わせて使用できます。
PHA は皮膚への放出が遅く、刺激性が低いため、皮膚が敏感になっている人の治療に適しています。保湿、角質除去、抗酸化作用を促進し、酒さの皮膚の治療にも使用できます。ラクトビオン酸とグルコノラクトンが目立ちます。
皮膚の健康のために現在注目されているもう 1 つのカルボン酸は、私たちの体内に自然に存在し、結合組織に多く含まれるヒアルロン酸です。この酸は、コラーゲンの生成を刺激するだけでなく、組織の水分を保ち、関節の潤滑を保つため、水分保持の役割を果たします。
しかし、年月が経つにつれて、ヒアルロン酸の生成が減少し、皮膚のしわ、表情跡、ボリュームの減少が生じ、さらに皮膚のサポートと弾力性に重要なタンパク質であるコラーゲンも減少します。
EDTA は最も使用されている化粧品成分の 1 つで、ほぼすべてのシャンプーに含まれています。これはキレート作用、つまり化粧品の安定性や外観に影響を与える可能性のある金属イオンを封鎖し、他の成分との干渉を防ぐ能力があることで知られています。また、水が硬いとシャンプーや石鹸の洗浄効果や泡立ち効果が低下するため、水の硬度を下げるためにも使用されます。したがって、EDTA は匂い、色の変化、自然摂取物の劣化、物質の不活化、ビタミンの酸化を防ぎます。
カルボン酸と人体
カルボン酸について話すとき、私たちの体に不可欠な 2 つの化学構造、アミノ酸と脂肪酸について考える必要があります。
アミノ酸
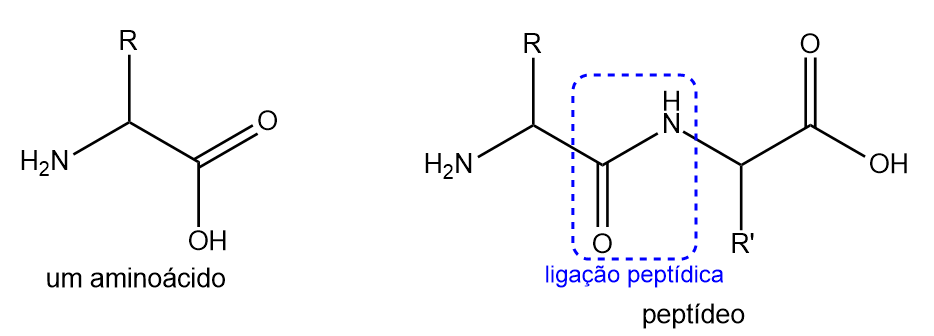
アミノ酸は、その構造内にアミン基とカルボン酸基が存在することを特徴とする化合物群を構成します。アミノ酸は互いに結合して、ペプチド結合としても知られるアミド結合によって結合された、いわゆるペプチドを形成することができます。
ペプチドは天然のポリマーであり、アミノ酸をモノマーとして含むため、数十個のアミノ酸が結合して形成されるペプチド(いわゆるポリペプチド)が存在します。 40~4000個のアミノ酸から構成されるポリペプチドはタンパク質として知られています。
タンパク質は生物にとって重要な機能を持っており、現在2,800万以上のタンパク質が知られています。
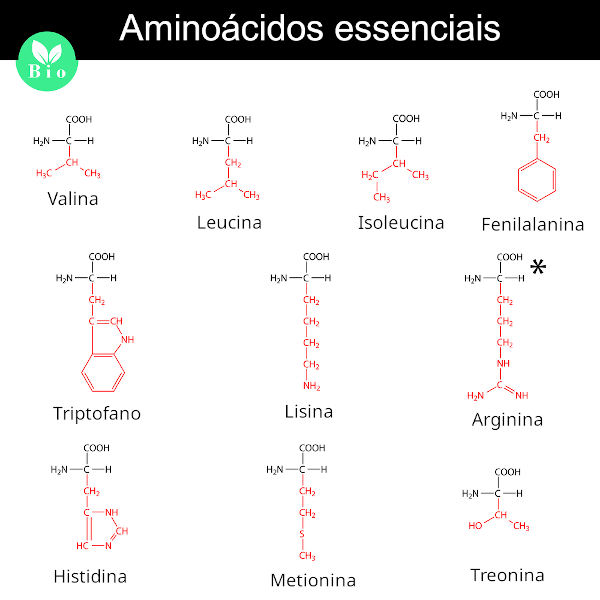
必須アミノ酸は10種類ありますが、これらは私たち人間によって合成されず、食事から摂取する必要があります。摂取しなければ、私たちの機能に不可欠ないくつかのタンパク質を合成することができません。
必須アミノ酸は、バリン、ロイシン、イソロイシン、スレオニン、メチオニン、リジン、フェニルアラニン、ヒスチジン、トリプトファン、アルギニンです。
脂肪酸
脂肪酸は、末端にカルボキシル基を持つ長い直鎖炭素鎖を特徴とする脂質です。この構造により、水などの極性溶媒にはほとんど溶けません。これらは自然界に存在し、アセテート単位(炭素原子数 2 つ)から生成されるため、常に偶数の炭素数を持ちます。
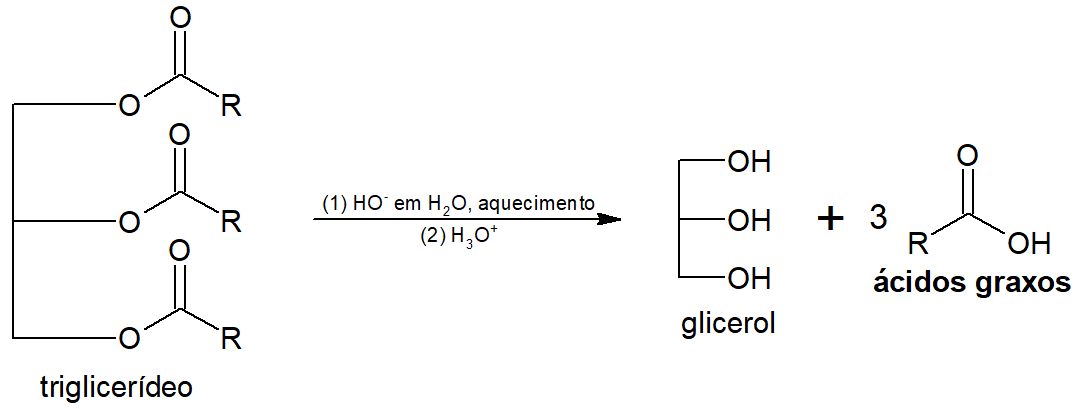
脂肪酸は、脂肪または油 (トリグリセリド) の加水分解から得られます。
脂肪酸には、飽和、不飽和 (炭素間に 1 つの二重結合がある)、または多価不飽和 (炭素間に 2 つ以上の二重結合がある) があります。脂肪酸に天然に存在する二重結合はシス配置になっています。
最もよく知られている脂肪酸は、いわゆるオメガ (3、6、9) です。この番号付けは、カルボン酸官能基を含まない脂肪酸の末端から数えて最初の二重結合を指します。
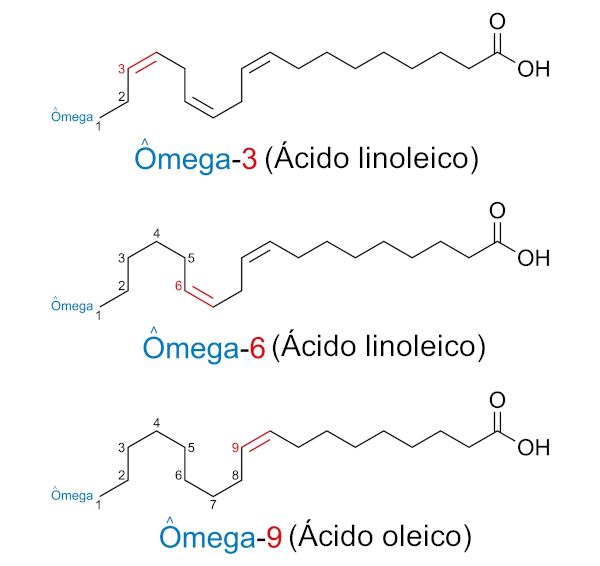
オメガ 3、オメガ 6、およびオメガ 9 酸は、人間が合成できないため、哺乳動物にとって必須の脂肪酸です。したがって、それらは私たちの体に不可欠であるため、食事から摂取する必要があります。たとえば、オメガ 3 酸は心臓発作による突然死のリスクの低下と関連しています。ストレスの多い状況では心臓が加速し、その心拍数が致命的になる可能性があります。このようにして、オメガ-3 は心臓の細胞膜に取り込まれ、心拍リズムの安定化に役立ちます。
カルボン酸反応
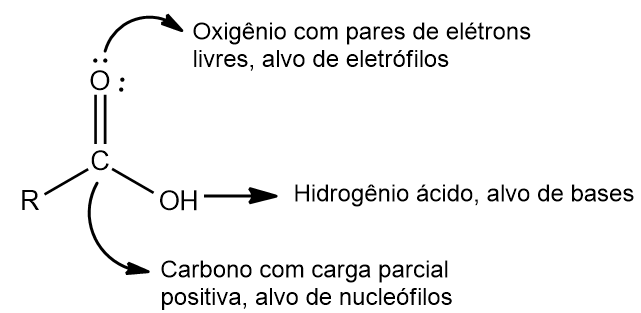
次の図に示すように、カルボン酸にはカルボキシル基にいくつかの反応部位があります。
カルボキシル炭素は求核置換反応を受けやすいですが、それはカルボン酸が結合している (イオン化していない) 場合に限られます。イオン化すると、酸素のマイナス電荷によって求核剤の接近が妨げられるためです。
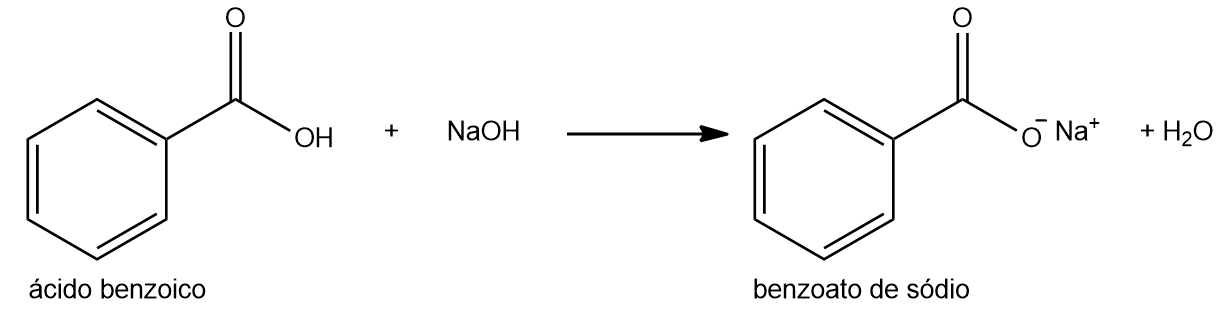
カルボン酸と強塩基の反応
それらはカルボン酸の塩を形成します。使用される塩基は通常、NaOH または KOH です。
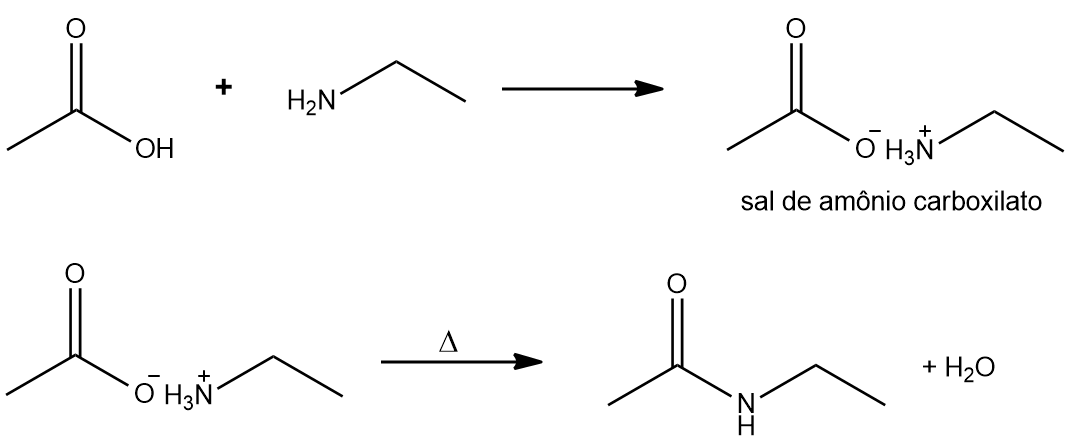
カルボン酸とアミンの反応
それらはカルボン酸アンモニウム塩を形成します。このような塩は加熱するとアミドを形成します。
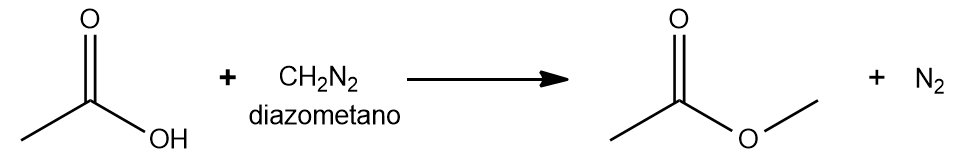
ジアゾメタンによるエステル化
ジアゾメタン (CH 2 N 2 ) はカルボン酸と迅速に反応してメチルエステルを形成します。
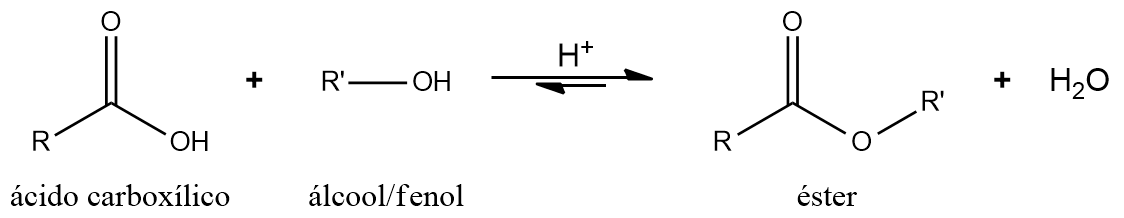
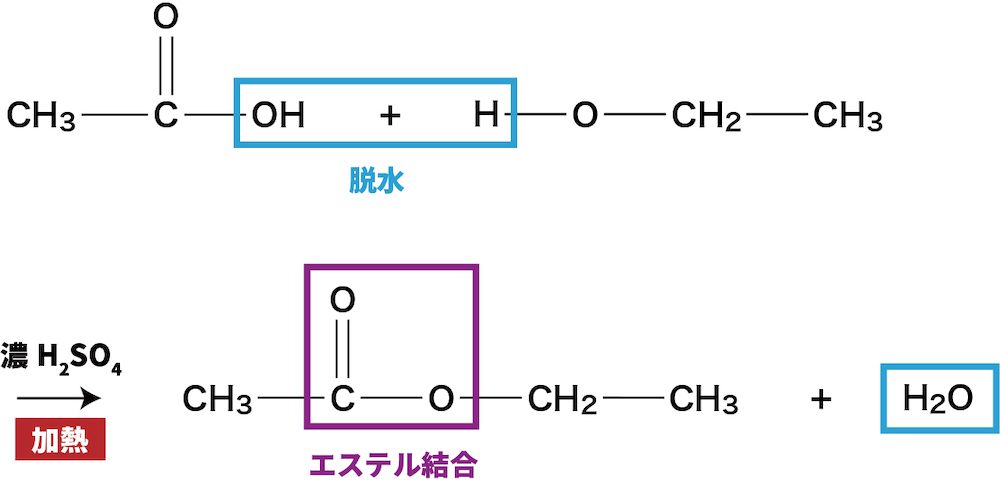
酸触媒によるエステル化
フィッシャーエステル化としても知られるこの反応は、触媒として強酸を使用したカルボン酸とアルコールまたはフェノールの反応で構成されます。この反応により、主生成物としてエステルが生成されます。
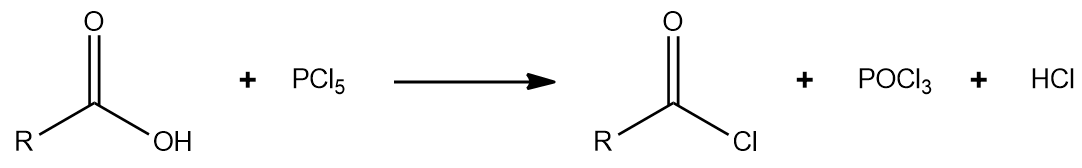
カルボン酸と五塩化リンの反応
このような反応では酸塩化物が生成されます。
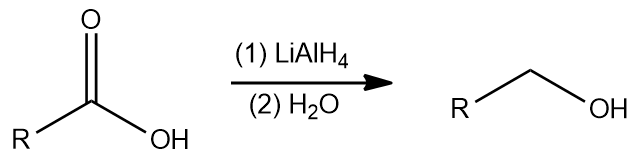
カルボン酸の第一級アルコールへの還元
LiAlH 4などの強力な還元剤を使用すると、カルボン酸を第一級アルコールに還元することができます。
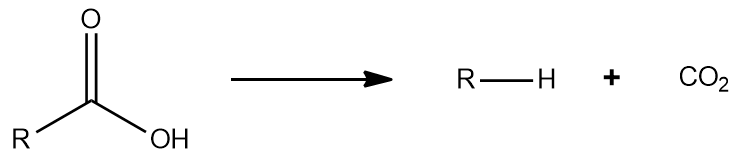
脱炭酸
カルボン酸による CO 2の損失からなる反応。二酸化炭素の安定性にもかかわらず、一般に、脱炭酸が適時に起こり有用となるためには、カルボン酸鎖に特別な基が存在する必要があり、そうでないと脱炭酸は非常に遅く、実行が困難です。
カルボン酸の塩
無機塩基やアミンなどの塩基性化合物と反応すると、カルボン酸がカルボン酸塩(またはカルボン酸の塩)を形成する可能性があることは以前から認識されていました。無機化学と同様に、その命名法では、カルボン酸の「-ic」が塩の「-ato」に置き換えられます。
ナトリウム塩とカリウム塩は、イオン部分の極性が高いため、長鎖カルボン酸であっても水に可溶です。実際、長鎖のナトリウム塩とカリウム塩は石鹸の主成分であり、最終製品では界面活性剤として機能します。
イオン部分は、カルボン酸で行われる従来の共有結合相互作用よりも強力なイオン相互作用およびイオン双極子相互作用を可能にするため、融点と沸点も上昇します。カルボン酸塩について詳しくは、ここをクリックしてください。