ヒドロキシルは、アニオン (-OH – ) またはラジカル (-OH) として機能する化学式 –OH を持つ官能基です。無機塩基は、水溶液中で解離し、OH –イオンを放出する物質として定義されます。ヒドロキシルイオンの存在は、培地のpH値の上昇に寄与します。いくつかの有機化合物は炭素鎖に結合したヒドロキシル基を持ち、原子の配置に従って異なる官能基の一部を形成します。アルコール、フェノール、カルボン酸は、-OH 構造を持つ有機官能基です。
ヒドロキシルについてのまとめ
ヒドロキシルは、式 –OH を持つ化学基です。
ヒドロキシルはアニオンまたはラジカルの場合があります。
無機塩基はヒドロキシルによって形成され、解離プロセス中に水中に放出される可能性があります。
ヒドロキシルイオン (-OH – ) の存在は、溶液の pH 値の上昇に寄与します。
アルコール、フェノール、カルボン酸など、一部の有機化合物はその構造内にヒドロキシル基を持っています。
ヒドロキシルとは何ですか?
ヒドロキシルまたはオキシドリルは、共有結合で結合した酸素原子と水素原子で構成される、化学式 –OH を持つ官能基です。
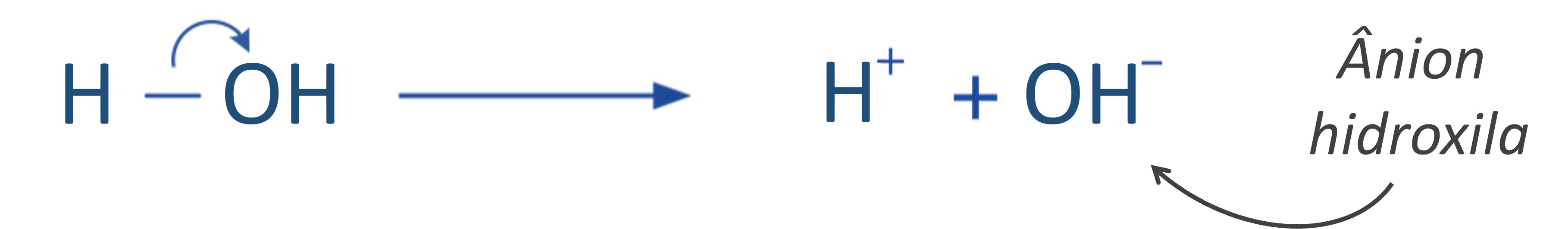
ヒドロキシルが負の電荷を持っている場合、それはヒドロキシルアニオン (-OH ‑ ) として知られます。負電荷は、アニオン形成時に化学結合のヘテロリシス的切断によって酸素電子圏に収容された追加の電子に由来します。
水分子の不均一破壊におけるヒドロキシルアニオンの形成を見てください。
ヒドロキシルアニオンは、基本的な無機機能のアレニウスの定義に関与しているため、無機化学における重要な研究対象です。有機化学では、ヒドロキシル基は有機官能基であるカルボン酸、アルコール、フェノールを構成します。
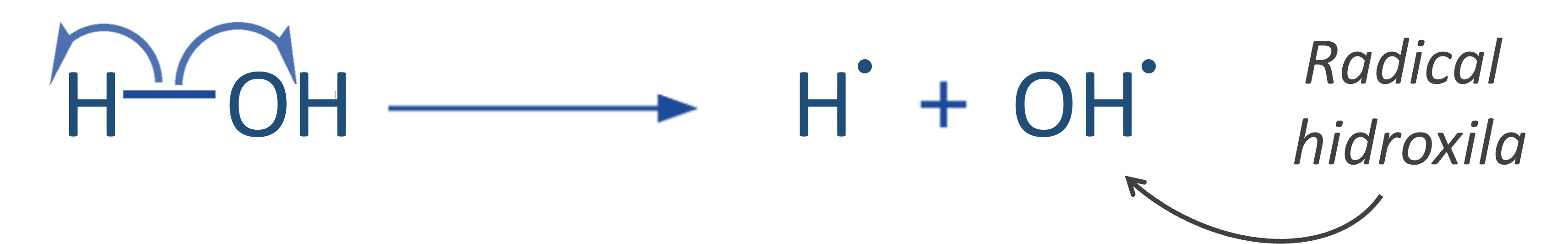
この官能基のもう 1 つの発生形態は、ヒドロキシル ラジカル (‧OH) の形です。これは、結合のホモリシス切断によって形成される種であり、結合内で共有される電子が 2 つの原子間に均等に分配されます。
ヒドロキシルラジカルは非常に反応性が高く、寿命が短いです。これらのラジカルが生体に存在すると、脂質、タンパク質、アミノ酸と反応して細胞に損傷を与えるため、通常は有害です。
アレニウス塩基とヒドロキシル
酸と塩基の化学反応を説明するにはさまざまな理論があります。酸塩基理論を最初に定式化した学者は、1884 年にスヴァンテ アレニウスでした。彼にとって、塩基または水酸化物は、水中でイオン解離を受け、唯一の陰イオンとしてヒドロキシル アニオンを放出する物質です。したがって、塩基は水溶液中の –OH –イオンの量を増加させることができる物質です。

水溶液中のヒドロキシルイオンの濃度は、溶液のpH測定に干渉します。 –OH –イオンの量が多いほど、pH 値が高くなり、塩基性またはアルカリ性が高いことを意味します。
こちらもご覧ください:アレニウス、ブレンステッド-ローリー、ルイスの酸塩基理論
有機化合物とヒドロキシル
有機化合物は官能基に応じて分類されます。一部の官能基はヒドロキシル –OH によって形成されます。
ヒドロキシル基の存在により、分子は隣接する分子と水素結合型の分子間相互作用を確立することができ、それらの間の静電引力が強化されます。この現象は、同じ官能基を持たない分子に関連して、化合物の融解温度と沸点を上昇させます。
有機化合物は水への溶解度が低いですが、構造中に水酸基を持つと水に溶けやすくなります。
→ 有機酸
弱酸とみなされる有機酸は、基本的には炭素鎖(アルキルラジカル) に結合したカルボキシル基 (-COOH) の存在を特徴とするカルボン酸です。

これらの化合物の酸性は、脱プロトン化プロセス、つまり溶液への水素(ヒドロキシルに結合)の放出に由来し、媒体中の H +イオンの濃度が増加し、媒体がより酸性になります。
この現象は、酸素原子と水素原子の電気陰性度の差が大きく、酸素原子と水素原子の間の化学結合を弱める要因によって起こります。酸素の電気陰性度が高まると、酸素は結合内の電子を引き寄せることになり、H +イオンが遊離したままになります。
カルボキシル基の場合、2 つの酸素原子の存在により電子にさらに大きな引力が働き、脱プロトン化がより有利になります。

→ アルコール
アルコールは、炭素鎖の飽和炭素原子にヒドロキシルが結合した有機官能基です。
アルコールは、鎖の末端を占め、一級炭素に結合している場合、一級アルコールとして分類できます。ヒドロキシル基は炭素鎖に沿って存在することもあり、それぞれ同じ名称の炭素に結合している場合は、第二級または第三級アルコールとして分類されます。

アルコールも、有機酸について説明した脱プロトン化プロセスを受ける可能性があります。
→ フェノール類
フェノールは、ヒドロキシルがベンゼン環に直接結合している有機官能基です。
問題.jpg)
フェノールはアルコールに似ていますが、水酸基に属する水素が脱プロトン化しやすいことから、アルコールに比べて酸性度が高いなど、異なる特性を持っています。
→ エノール
エノールは、ヒドロキシルが不飽和炭素に結合し、二重結合を形成する有機官能基です。

これらの化合物は不安定で、ケトンやアルデヒドなどの他の化合物に容易に変換され、互変異性として知られる動的平衡を確立します。
ヒドロキシルの用途
ヒドロキシルは有機および無機の両方の多くの物質に存在するため、その用途は非常に多様です。
無機塩基を考慮すると、ヒドロキシルは、次のような産業的および経済的関連性のあるいくつかの塩基の組成の一部です。
水酸化ナトリウム (NaOH) :強力洗浄製品に使用されます。
水酸化カリウム (KOH):石鹸や洗剤の製造、電池産業、肥料の製造に使用されます。
水酸化カルシウム (Ca(OH) 2 ):水および排水処理プラント、土木建設、土壌酸性度補正に使用されます。
水酸化マンガン (Mg(OH) 2 ):便秘薬であるマグネシアミルクの組成に使用される弱塩基。
ヒドロキシルを含む有機化合物の中で、カルボン酸は弱酸であり、さまざまな機能を備えているため、際立っています。
酢酸 (CH 3 COOH) :酢の主成分で、調味料や保存料として使用されます。
アセチルサリチル酸 (C 9 H 8 O 4 ) :アスピリンを含む多くの薬剤の有効成分。
クエン酸 (C 6 H 8 O 7 ):柑橘類に含まれる化学物質。
アルコールには次のようなさまざまな用途があります。
エタノール (CH 3 CH 2 OH) :バイオ燃料、洗浄剤、殺菌剤として使用され、アルコール飲料にアルコール度が割り当てられます。
メタノール (CH 3 OH) :さまざまな工業プロセスで溶媒として使用され、ホルムアルデヒド製造の試薬として、香水、バイオディーゼルおよび医薬品の製造で使用されます。
フェノールの中で最も有名な物質は次のとおりです。
フェノール (C 6 H 6 OH):現在、染料、樹脂、クレゾール、化学試薬、アセチルサリチル酸の製造に使用されています。
ピクリン酸 (2,4,6-トリニトロフェノール):火傷を治療するための軟膏や、パンのハンドルなどに使用される軽量で耐熱性のポリマーであるベークライトの製造に使用される化合物。
バニリン (C 8 H 8 O 3 ):バニラエッセンスとしてよく知られています。
ヒドロキシル、カルボニル、カルボキシルの違い
ヒドロキシル:酸素と水素原子の間の共有結合によって構成される官能基であり、塩基および有機官能基であるアルコール、カルボン酸、フェノールおよびエノールに存在します。
カルボニル:二重結合を介して酸素原子に結合した炭素原子によって形成される有機官能基です。カルボニルには水酸基がありません。カルボニルは、ケトン、カルボン酸、アルデヒド、エステル、アミドなどのさまざまな有機官能基に存在します。

カルボキシル:同じ炭素原子上のヒドロキシル基とカルボニル基の結合によって形成される有機基です。カルボキシルは有機カルボン酸官能基で発生します。