「化学元素の分類」のテキストに記載されているように、非金属 (または非金属) は、上の図に示されている 11 の化学元素、つまり炭素 (C)、窒素 (N)、リン (P)、酸素 (O) に対応します。 )、硫黄 (S)、セレン (Se)、フッ素 (F)、塩素 (Cl)、臭素 (Br)、ヨウ素 (I)、アスタチン (At)。
これらの元素は、化学種間で電子交換が起こる酸化還元反応に関与します。これらの反応は、単体 (1 種類の化学元素のみで形成される) が複合物質 (複数の元素で形成される) から新しい単体を「置き換える」ため、単純交換反応または置換反応とも呼ばれます。よりよく理解するために、この変位がどのように発生するかを示す次の一般的な図を示します。
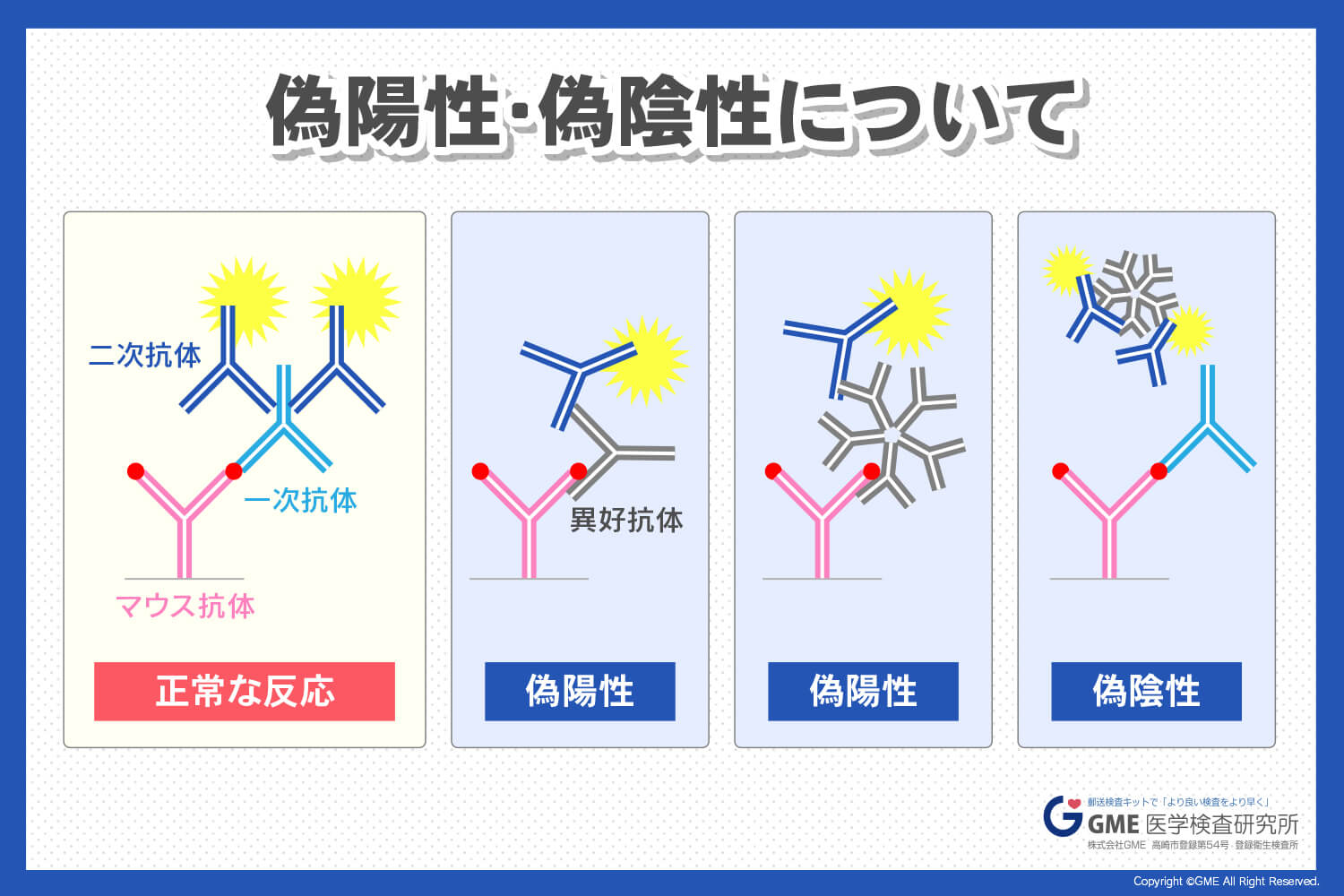
A + BC → A B + C
A が複合物質から元素 C を置き換えていることに注目してください。しかし、このような反応が実際に起こるためには、単体を構成する非金属が複合物質に存在する非金属よりも反応性が高い必要があります。
非金属の反応性は、これらの元素が電子を獲得して陰イオン (イオンまたは負に帯電した化学種) を形成する傾向に対応します。これは、非金属が電気陰性元素である、つまり電子を引き付ける傾向が高いために発生します。したがって、非金属の電気陰性度が大きいほど、反応性が高くなります。
たとえば、塩化カリウムをヨウ素と接触させたとしましょう。

KCl (水溶液) + I 2(水溶液) → ?
この反応は起こるのでしょうか?ヨウ素は塩化カリウムから塩素を置き換えますか (2 KCl (aq) + I 2(aq) → 2 KI (aq) + Cl 2(aq) )?
この反応は、ヨウ素が塩素よりも反応性が高い場合にのみ発生します。非金属の反応性の次数は、元素の電気陰性度を測定することによって実験的に決定されました。電気陰性度を測定する方法はいくつかありますが、最もよく知られ使用されている方法は、科学者ライナス・ポーリングによって決定された方法です。その値は次の画像に示されています。
周期表におけるポーリングの電気陰性度の値
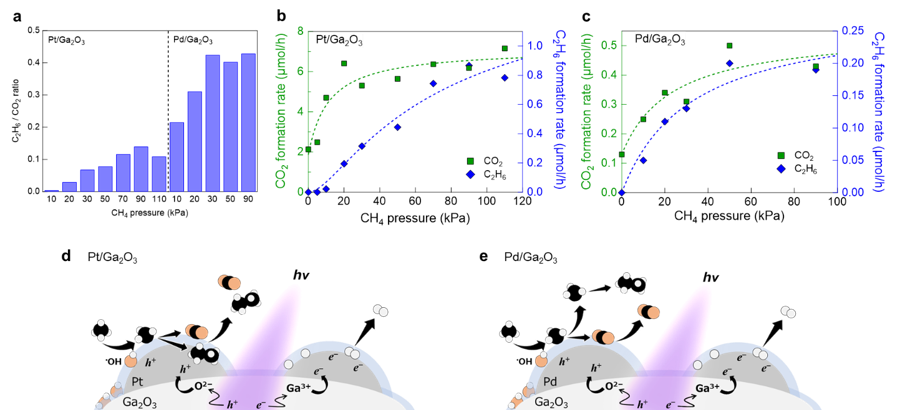
これらの値に基づいて、最も処理される傾向にある最も電気陰性度の高い元素の電気陰性度キューも作成されました。
F > O > N > Cl > Br > I > S > C > P > H
これらの元素の電気陰性度の値をそれぞれ参照してください。
4.0 > 3.5 > 3.0 > 3.0 > 2.8 > 2.5 > 2.5 > 2.5 < 2.1
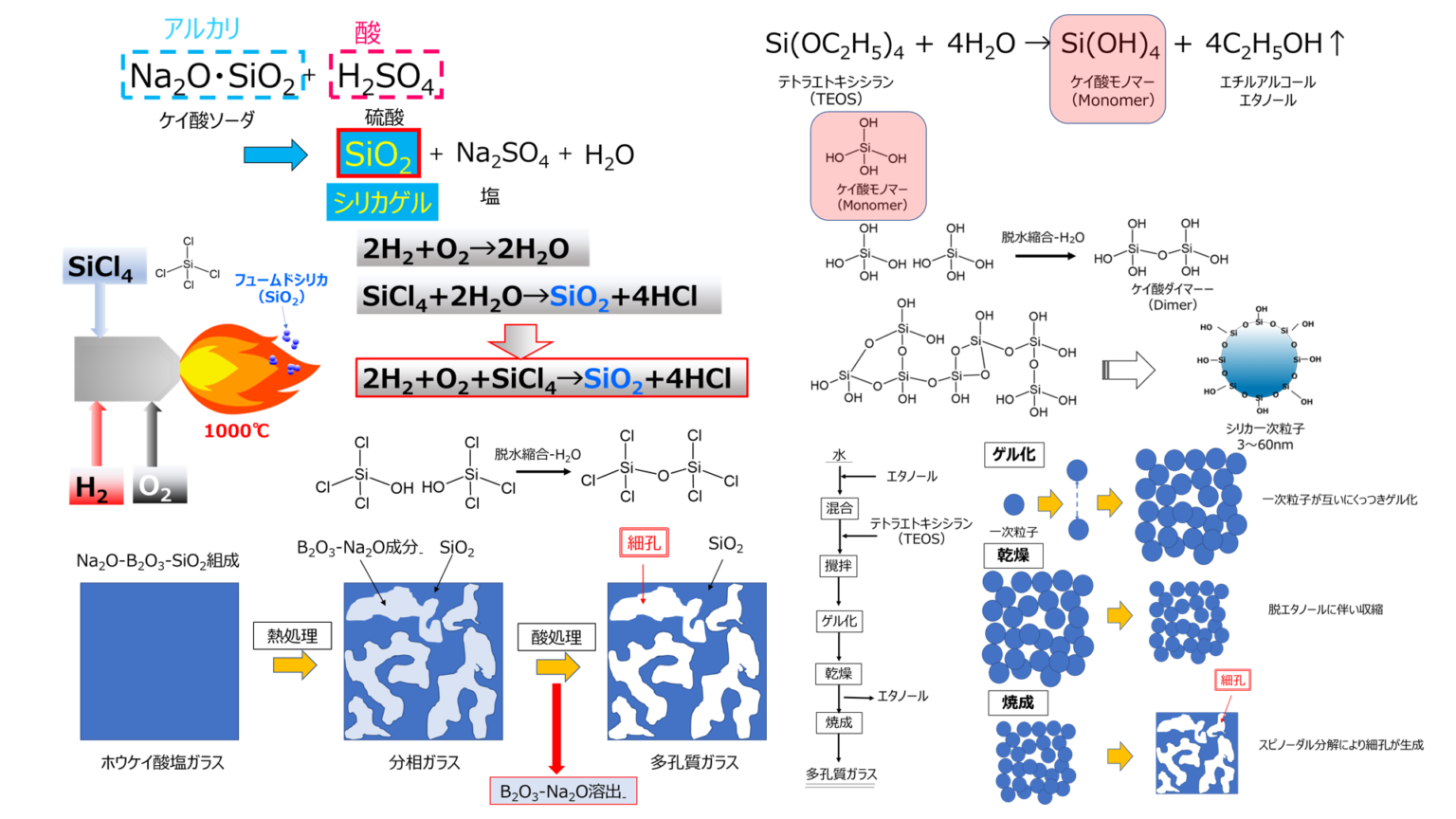
水素は非金属ではありませんが、その反応性は比較の目的でこの行に配置されるのが一般的です。
この電気陰性度の行を装飾するための一種の「トリック」があり、それは次の文で与えられます。 昨日 いいえ クラブ、 ブライゲイ 私 さあ、どうぞ ランニング のために 病院“ 。各単語の最初の文字は、反応性キューに表示される正確な順序で要素のシンボルに対応します。
非金属の反応性の順序がわかったので、塩化カリウムとヨウ素の反応が起こるかどうかを言うことができます。ヨウ素 (電気陰性度 2.5) は塩素 (電気陰性度 3.0) よりも反応性が低いことに注意してください。したがって、このような単純な交換反応は起こりません。
KCl (水溶液) + I 2(水溶液) → 発生しない

一方、塩素水とヨウ化カリウムの反応の場合、塩素はヨウ素よりも反応性が高く、ヨウ素を置換できるため、反応が起こります。見て:
2 KI (水溶液) + Cl 2 (水溶液) → 2 KCl (水溶液) + I 2 (水溶液)
塩素水とヨウ化カリウムはどちらも無色の溶液を形成するため、この反応の発生を視覚化することができます。しかし、反応させると、ヨウ素の生成により茶色が観察されます。
塩素水とヨウ化カリウムの酸化還元反応におけるヨウ素沈殿物の形成

これらの元素が関与する反応が実際に起こるかどうかを判断する方法については、 「金属の反応性」というテキストも参照してください。
関連するビデオレッスン:


