重量の法則は、ラヴォアジエの質量保存の法則やプルーストの定数比例の法則など、反応中に存在する物質の質量を数学的に関連付けたものです。
体積法則は、化学反応に関与するガスの体積を指し、重量法則を補完します。最も重要な体積法則は、1808 年にジョセフ ゲイ リュサック (1778-1850) によって作成されたもので、体積結合の法則またはゲイ リュサックの体積法則と呼ばれます。いくつかの実験を実施し、化学反応におけるガスの体積を測定した後、彼は次のような結論に達しました。
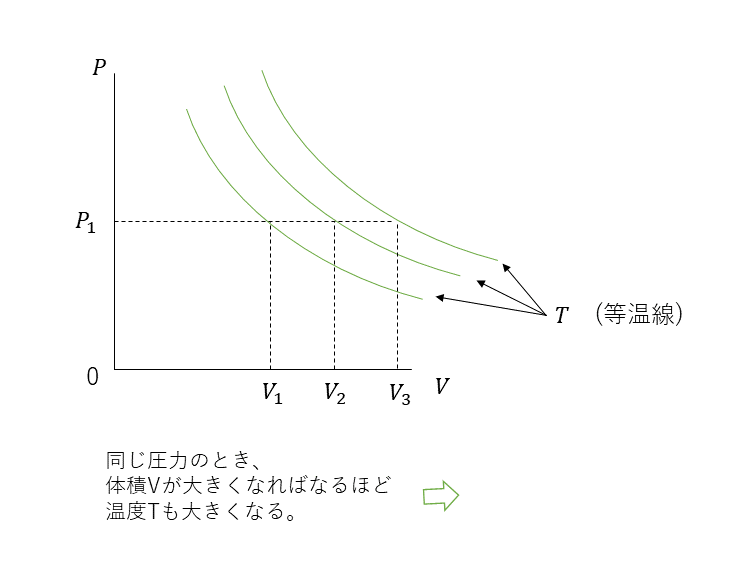
「同じ温度と圧力の条件下では、化学反応の反応物と生成物のガスの体積は常に小さい値と整数の間の関係になります。」
たとえば、水蒸気の形成を伴う、水素と酸素ガスの反応を考えてみましょう。ゲイ=リュサックは、この反応では常に 2 体積の水素が 1 体積の酸素と反応し、2 体積の水が生成されることに気づきました。

水素+酸素→水
1回目の実験: 2L 1L 2L
実験2: 10L 5L 10L
実験3: 18L 9L 18L
4回目の実験:40L 20L 40L
すべての場合において、体積の比率は、整数と小さな数値の関係 ( 2 : 1 : 2 ) にあることに注意してください。どの種類の反応でも、体積間には常にこのような関係がありますが、その割合は変化します。別の例を参照してください。
:max_bytes(150000):strip_icc()/GettyImages-654393380-5a412f6d7bb28300374e1199.jpg)
水素+塩素 → 塩酸ガス
1回目の実験: 1L 1L 2L
実験2:10L 10L 20L
実験3:15L 15L 30L
4回目の実験:40L 40L 80L
この場合、ガスの体積の比率は1 : 1 : 2で与えられることに注意してください。

それまで受け入れられていた原子理論は、物質は原子と呼ばれる小さな粒子によって形成され、それは巨大で分割不可能であるというダルトンの原子理論でした。この理論によれば、原子の数は化学反応中に一定に保たれ、生成物の体積は反応物の体積の合計を表す必要があります。
前述の最初の化学反応ではこれは起こらないことに注意してください。反応物の比率が 2:1 であるため、生成物の体積は 3 (2 + 1) に等しくなるはずですが、実験的には 2 に等しくなります。これが起こると、体積の収縮があったと言えます。このようにして、ゲイ=リュサックの法則がダルトンの原子理論に適用されました。
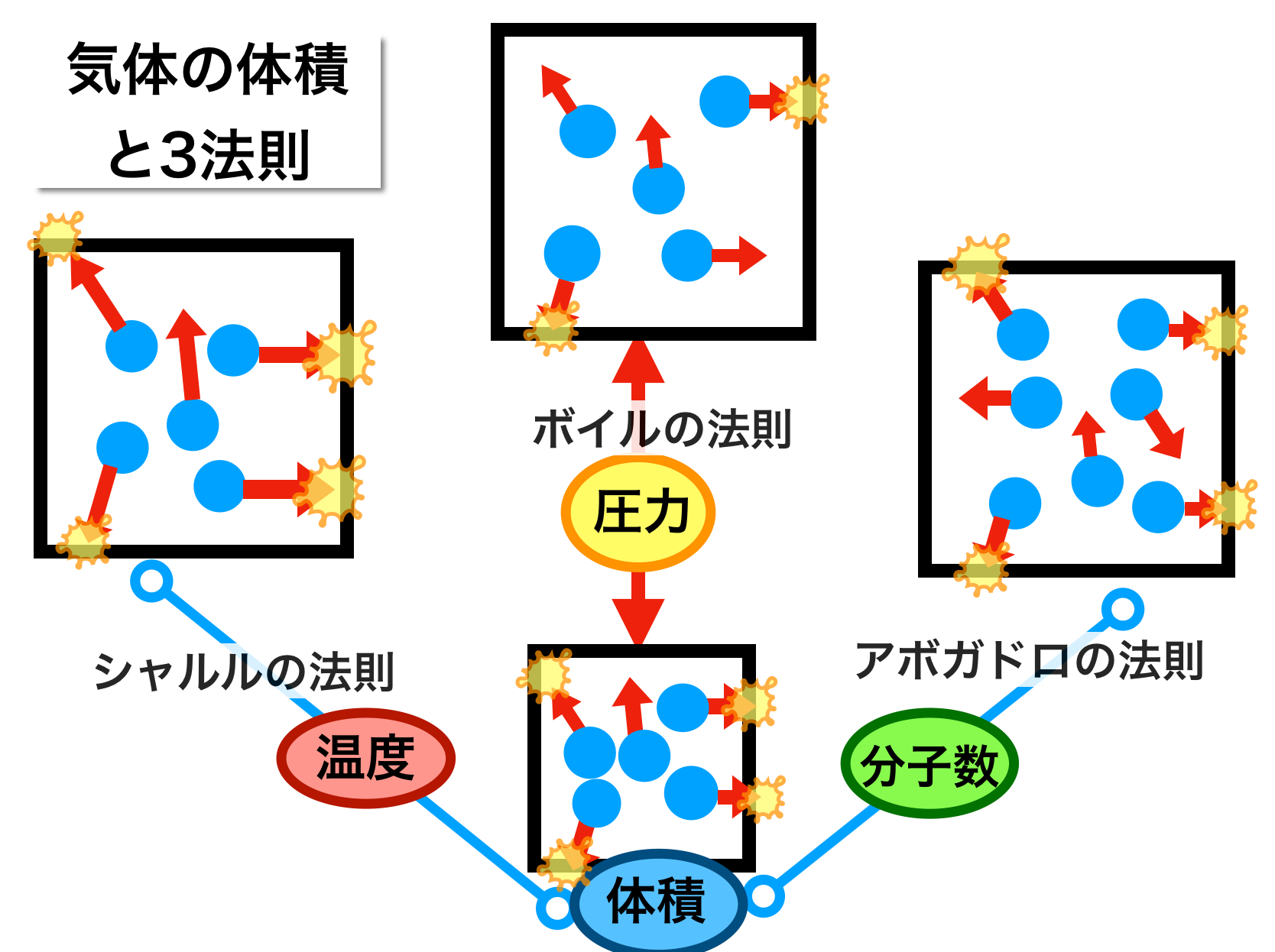
しかしその後、1811 年に科学者のアメデオ アボガドロが、なぜこれが起こったのかを説明しました。アボガドロの仮説または原則は、テキスト「アボガドロの法則」で詳しく見ることができますが、次のように述べています。 同じ温度と圧力条件下では、どの気体もモルまたは分子単位で同じ量の物質を持っています。 」
これは、ガスが常に孤立した原子によって形成されるわけではなく (これは希ガスの場合にのみ起こります)、むしろ分子によって形成されることを意味します。したがって、これらの分子内の原子は化学反応中に再結合し、観察される割合を説明します。

たとえば、水の生成反応の場合に何が起こるかを見てください。水素ガスと酸素ガスの各分子は 2 つの原子で形成されますが、各水分子は 3 つの原子 (水素 2 個と酸素 1 個) で形成されます。したがって、 2 つの水素分子 (4 つの原子) が1 つの酸素分子 (2 つの原子) と反応して、 2 つの水分子 (合計 6 つの原子が得られます) が生成されることがわかります。

このようにして、体積間の比率と反応に関与した原子の数の両方が維持されました。
このことから、アボガドロは、同じ温度と圧力にある限り、気体が何であっても、同じ体積の気体は同じ数の分子を持っているという別の重要な結論に導きました。上記のケースでこれを確認します。 H 2の体積は H 2 O の体積と同じであり、それらが持つ分子の数も同じであることがわかります。

.jpg)