理想気体とは、そのすべての粒子または分子が完全に弾性的に衝突し、分子間力が存在しない気体です。このタイプの気体では、内部エネルギーは各粒子の運動エネルギーの合計に相当します。さらに、圧力、体積、温度という 3 つの状態変数を通じて特徴付けることができます。
ガスとは何ですか?
気体は物質の物理状態の 1 つです。十分に高い温度では、室温では固体である元素も気体になるため、気体とは気体状態にあるあらゆる物質を指します。
ガスには定義された形状がないため、その容器の形状に従います。さらに、その粒子は高速で移動し、液体や固体などの物質の他の物理状態に比べて互いに遠く離れています。


理想的なガス特性
理想気体の主な特徴は、粒子間に引力や斥力が存在せず、粒子同士、またはそれらを含む容器の壁と弾性的に衝突することです。さらに、理想気体では分子が占める空間はごくわずかであることが理解されています。
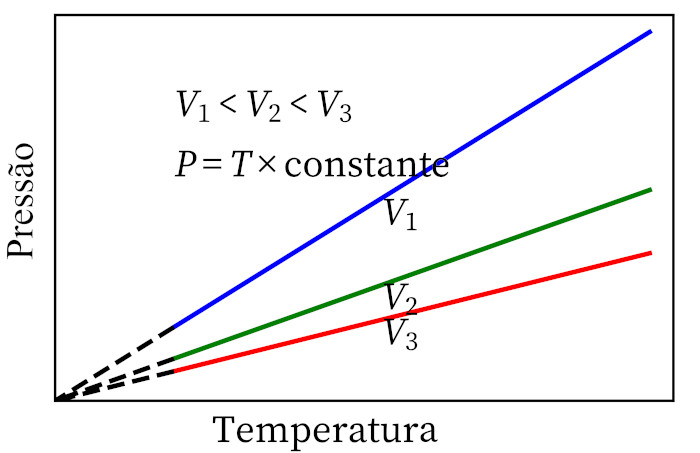
歴史を通じて行われた一連の実験は、理想気体で予想される特性に似た特性を持つ一定量の気体は、非常に単純な法則に従うことを示しています。理想気体が密閉された硬い容器(一定容積)内で加熱されると、気体の圧力はその温度と同じ割合で増加します。言い換えれば、このような条件下では、温度と圧力は直接変化します。 比例。
要約すると、理想気体には次の特徴があると言えます。
- 気体分子間に引力または反発力が存在しない。
- 完全に弾性のある。
- 空間を占有せず、無秩序に移動する粒子。
実際には存在しませんが、理想気体は、ほとんどの現実の気体が低圧と高温にさらされる場合の挙動をよく表していることを知っておくことが重要です。

ガス法
気体法則は、理想気体が受ける状態変化を指します。主なガス変化は、17 世紀から 19 世紀にかけて科学者によって作成されたこれらの法則によって説明されます。
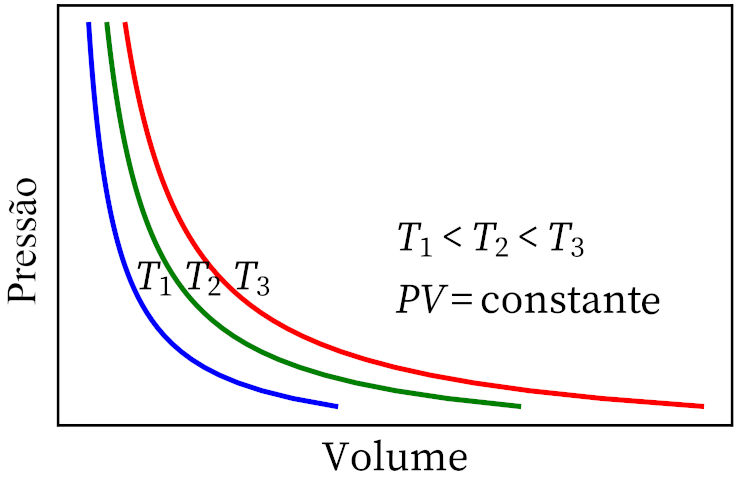
- ボイルの法則: 等温変換では、気体の圧力と体積は互いに反比例し、その積は一定であると述べています。
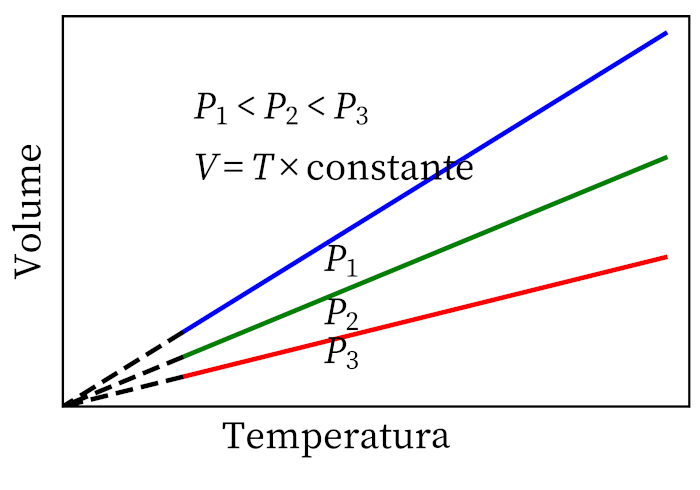
- ゲイ・リュサックの法則:一定の圧力下では、気体の体積と温度は比例するため、それらの比率は常に一定であると述べています。
- シャルルの法則: 気体が一定の体積変化を起こすとき、その圧力と温度は比例するため、これら 2 つの量の比は常に同じ測定値になります。

理想気体の法則
理想気体の法則では、気体の圧力と体積の積は気体の温度に比例すると規定されています。この場合の比例定数は、理想気体の普遍定数だけでなく、気体に含まれるモル数によって決まります。理想気体の法則は次のように表されます。
P – 圧力 (atm、Pa)
V – 体積 (l、m3)
n – モル数 (mol)
R – 汎用理想気体定数 (0.082 atm.l/mol.K または 8.3 J.mol/K)
T – 熱力学温度 (K)